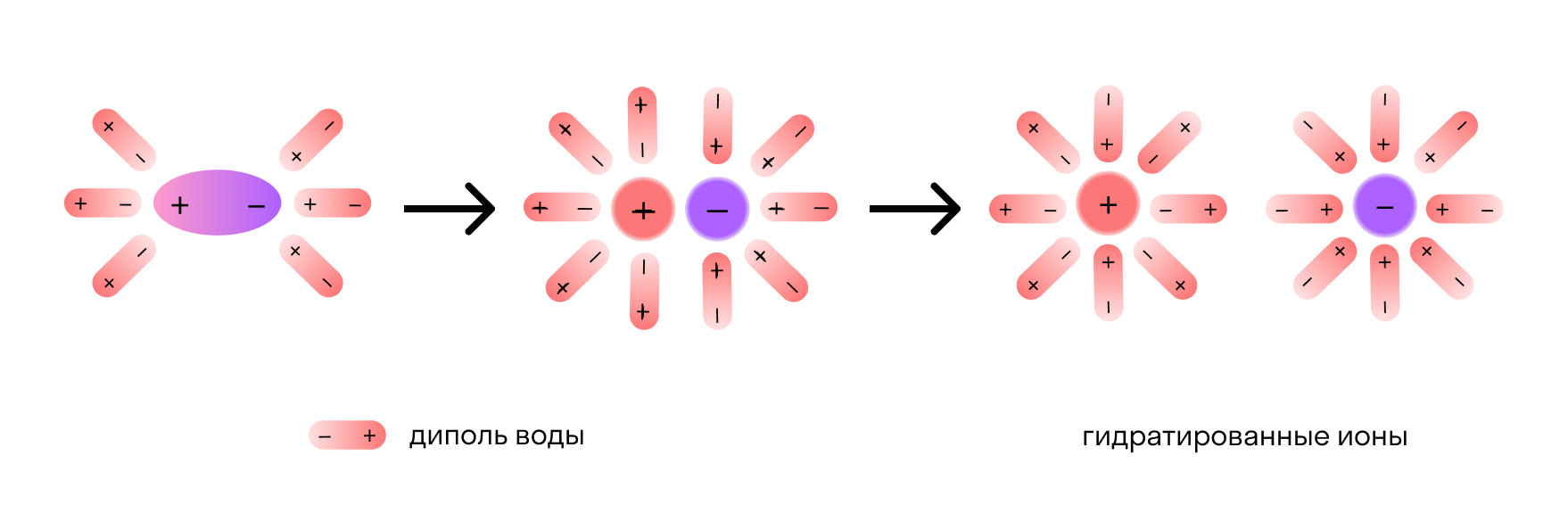
Деление ионов — это физический процесс, в котором ионы, находящиеся в растворе, разделяются на гидратированные и негидратированные формы. Гидратированные ионы окружены молекулами воды, что влияет на их свойства и поведение в растворе. Понимание этого процесса играет важную роль в многих областях науки, включая химию, физику и биологию.
Гидратированные ионы, также известные как гидраты, образуются в результате взаимодействия ионов с молекулами воды. Это образует оболочку вокруг иона, состоящую из молекул воды, которая помогает стабилизировать его заряд и облегчает его перемещение в растворе. Гидратированные ионы обычно обладают некоторыми уникальными свойствами, такими как изменение растворимости и возможность образования комплексов с другими веществами.
С другой стороны, негидратированные ионы находятся в свободном состоянии без оболочки воды. Они обладают свойствами, которые могут отличаться от гидратированных форм, их экспериментальное определение может быть трудным ввиду их высокой реакционной способности и возможности образования агрегатов в растворе. Исследования различных свойств негидратированных ионов очень важны для понимания их поведения в различных типах реакций в живых организмах и в окружающей среде.
Влияние деления ионов
Деление ионов играет важную роль во многих химических и физических процессах, так как оно влияет на свойства и наличие гидратированных и негидратированных ионов в растворе.
Гидратированные ионы, также известные как комплексные ионы, образуются при гидратации ионов растворителем, обычно водой. Гидратные оболочки окружают ионы, образуя структуры, которые влияют на их химические и физические свойства. Гидратация может увеличить положительный или отрицательный заряд иона, изменить его радиус и влиять на его реакционную способность.
Негидратированные ионы, или свободные ионы, не имеют окружающих гидратных оболочек и свободны от взаимодействий с растворителем. Они обладают свойствами, полностью определяемыми ионно-межионными взаимодействиями и электростатическими силами, и их поведение может отличаться от гидратированных ионов.
Влияние деления ионов на свойства и наличие гидратированных и негидратированных ионов может быть очень значительным. Оно может определять скорость реакций, растворимость веществ, проводимость электричества в растворе и многие другие химические процессы.
Понимание влияния деления ионов на гидратированные и негидратированные ионы является важным аспектом изучения химии и может быть полезным при решении различных практических задач, таких как разработка новых материалов, улучшение производства и оптимизация процессов хранения и транспортировки веществ.
В итоге, деление ионов играет ключевую роль в формировании свойств и наличия гидратированных и негидратированных ионов, а понимание этого влияния может быть полезным при решении различных химических и физических задач.
На свойства
Напротив, негидратированные ионы, не связанные с молекулами воды, имеют обычно более низкую энергию и структурную организацию. Они могут образовывать менее сложные структуры и показывать меньшую подвижность. Кроме того, негидратированные ионы могут более активно взаимодействовать с другими молекулами и ионами, что может влиять на их химические и физические свойства.
Таким образом, деление ионов на гидратированные и негидратированные играет важную роль в определении их свойств и влияния на окружающую среду. Взаимодействие с молекулами воды может существенно изменять энергетические и структурные характеристики ионов, что отражается на их химической активности и возможности вступать в реакции с другими веществами.
Разделение на гидратированные и негидратированные
Вода может гидратировать различные типы ионов, в зависимости от их полярности и размера. Гидратированные ионы могут быть как одно-, так и многоатомными. Гидратированные ионы образуют структуры, называемые гидратные сферы, которые могут быть катионами или анионами. Гидратация может изменять взаимодействие ионов друг с другом и окружающей среды.
С другой стороны, негидратированные ионы не образуют структур с водой и не имеют гидратных оболочек. Они обычно имеют меньшую растворимость в воде и могут образовывать соли с низким содержанием воды. Негидратированные ионы обладают свойствами, чтобы растворяться в органических растворителях, таких как этер и ацетон, в отличие от гидратированных ионов.
Разделение на гидратированные и негидратированные ионы имеет важное значение при изучении свойств ионов и их взаимодействия с окружающей средой. Понимание этого разделения помогает в определении физических и химических свойств ионов и использовании их в различных сферах научных исследований и промышленных процессов.
Изменение физических и химических характеристик
Деление ионов на гидратированные и негидратированные вещества оказывает существенное влияние на их физические и химические характеристики. Гидратированные ионы взаимодействуют с молекулами воды, что приводит к образованию гидратных оболочек вокруг них.
Это гидратирование ионов влияет на такие свойства вещества, как его растворимость, теплота растворения, электропроводность, оптические свойства и другие. Гидратированные ионы могут образовывать комплексные соединения с другими веществами, что также влияет на их химические характеристики.
С другой стороны, негидратированные ионы, не связанные с водой, имеют другие физические и химические свойства. Их растворимость и электропроводность могут быть существенно ниже, чем у гидратированных ионов. Также негидратированные ионы более склонны к реакциям соединения между собой и с другими веществами.
Изменение степени гидратации ионов может быть вызвано различными факторами, такими как температура, давление и концентрация вещества. Эти изменения могут иметь принципиальное значение для понимания свойств и реакций гидратированных и негидратированных ионов, а также применяться в различных областях химии и физики.
На наличие
Деление ионов на гидратированные и негидратированные имеет важное влияние на их свойства и наличие.
Гидратированные ионы представляют собой ионы, которые связаны с молекулами воды. Гидратированные ионы образуют структуру гидратной оболочки, когда молекулы воды окружают ионы, образуя гидратационную сферу вокруг них. В результате гидратации, ионы приобретают новые свойства и устойчивость в водных растворах.
Негидратированные ионы, наоборот, не связаны с молекулами воды и не образуют гидратационную сферу. Они не имеют гидратной оболочки и свойств, которые присущи гидратированным ионам.
Поэтому, наличие гидратированных и негидратированных ионов в растворе может значительно влиять на его физические свойства и реакционную способность. Гидратированные ионы обычно обладают большей подвижностью и устойчивостью в водных растворах, что может привести к более быстрому химическому взаимодействию и образованию новых соединений.
Таким образом, деление ионов на гидратированные и негидратированные играет важную роль в изучении их свойств и влияния на физико-химические процессы. Понимание этого явления позволяет более точно описывать и объяснять различные явления и реакции, происходящие в растворах и системах с участием ионов.
Влияние на растворимость
Деление ионов на гидратированные и негидратированные существенно влияет на растворимость соединений. При расщеплении соединения на ионы, происходит избирательное взаимодействие с молекулярными элементами растворителя.
Гидратированные ионы образуют сильные водородные связи с молекулами растворителя, что способствует их растворимости. Это связано с образованием гидратных оболочек вокруг ионов, которые снижают ионную силу и способствуют их лучшему растворению.
В свою очередь, негидратированные ионы не образуют таких сильных связей с растворителем, что ограничивает их растворимость. Это происходит из-за их большей зарядовой плотности и отсутствия образования гидратных оболочек.
Взаимодействие с другими веществами
Гидратированные и негидратированные ионы могут взаимодействовать с другими веществами и проявлять различные свойства в химических реакциях и соединениях.
Например, гидратированные ионы могут образовывать соли, кислоты или основания и участвовать в реакциях окисления-восстановления. Они могут также образовывать комплексы с различными лигандами, что влияет на их степень растворимости и активность.
Негидратированные ионы часто обладают более высокой активностью и реакционной способностью. Они могут образовывать ковалентные связи с другими атомами и молекулами, что позволяет им участвовать в различных химических реакциях.
Взаимодействие гидратированных ионов и негидратированных ионов с другими веществами также может приводить к образованию осадков или изменению физических свойств растворов, таких как вязкость или концентрация ионов.
| Вещество | Взаимодействие с гидратированными ионами | Взаимодействие с негидратированными ионами |
|---|---|---|
| Соль | Образование ионных связей | Образование ковалентных связей |
| Кислота | Протонирование или образование ионных связей | Протонирование или образование ковалентных связей |
| Основание | Образование ионных связей | Образование ковалентных связей |
| Лиганд | Образование координационных связей | Образование ковалентных связей |
Таким образом, деление ионов на гидратированные и негидратированные имеет важное значение при изучении их взаимодействия с другими веществами и определении их химических свойств и активности.
Вопрос-ответ:
Как деление ионов влияет на свойства гидратированных и негидратированных ионов?
Деление ионов может влиять на свойства гидратированных и негидратированных ионов в разных направлениях. Например, гидратированные ионы могут быть более подвижными и реактивными, чем негидратированные ионы. Это связано с тем, что гидратированные ионы обладают дополнительными молекулами воды, которые могут участвовать в химических реакциях. Однако, деление ионов также может приводить к изменениям в заряде и размере ионов, что в свою очередь может влиять на их свойства.
Какое влияние деление ионов оказывает на наличие гидратированных и негидратированных ионов?
Деление ионов может влиять на наличие гидратированных и негидратированных ионов. В некоторых случаях, деление ионов может привести к образованию гидратированных ионов, то есть ионов, которые связаны с молекулами воды. Это связано с тем, что вода является полюсным растворителем и способна образовывать водородные связи с ионами. В других случаях, деление ионов может привести к образованию негидратированных ионов, то есть ионов, которые не связаны с водой. Это может произойти, например, при высоких температурах или низкой концентрации воды.
Как деление ионов влияет на свойства гидратированных и негидратированных ионов в растворе?
Деление ионов может влиять на свойства гидратированных и негидратированных ионов в растворе. Например, гидратированные ионы могут образовывать комплексы с другими соединениями в растворе, что может влиять на их реакционную способность. Кроме того, гидратированные ионы могут образовывать ионные объединения, такие как соли, которые могут иметь специфические свойства, такие как растворимость, реакционную активность и электрохимическое поведение. Негидратированные ионы, напротив, могут проявлять свои свойства в виде самостоятельных частиц, например, как катализаторы химических реакций или как основные или кислотные центры в реакциях.
Какое влияние оказывает деление ионов на свойства гидратированных и негидратированных ионов?
Деление ионов влияет на свойства гидратированных и негидратированных ионов. Гидратированные ионы образуют гидратные оболочки вокруг себя, что влияет на их электрическую проводимость и взаимодействие с другими частицами. Негидратированные ионы не имеют гидратных оболочек и обладают другими свойствами, такими как реактивность и растворимость.
Что такое гидратированные ионы?
Гидратированные ионы — это ионы, которые образуют гидратные оболочки вокруг себя в растворе. Когда ион попадает в воду, молекулы воды ориентируются вокруг иона и образуют с ним слабую связь. Это приводит к образованию гидратной оболочки вокруг иона. Гидратированные ионы могут иметь другие свойства и взаимодействия, чем негидратированные ионы.
Какие свойства гидратированных и негидратированных ионов различаются?
Свойства гидратированных и негидратированных ионов могут различаться. Гидратированные ионы имеют гидратные оболочки, которые могут повлиять на их электрическую проводимость, растворимость и взаимодействие с другими частицами. Негидратированные ионы, не имеющие гидратной оболочки, могут обладать другими свойствами, такими как реакционная активность и способность образовывать соединения с другими частицами без учета влияния гидратации.
Может ли деление ионов повлиять на наличие гидратации?
Да, деление ионов может повлиять на наличие гидратации. Некоторые ионы имеют большую аффинность к воде и легко гидратируются, образуя гидратные оболочки вокруг себя. Другие ионы могут иметь меньшую аффинность к воде и гидратацию проводить слабо или не проводить вовсе. Таким образом, деление ионов может определять наличие или отсутствие гидратации в растворе.